تعميم رقم (63901/ع) وتاريخ 26-10-1439هـ
نص التعميم مكتوب
تعميم رقم (63901/ع) وتاريخ 26-10-1439هـ
السلام عليكم ورحمة الله وبركاته،،،
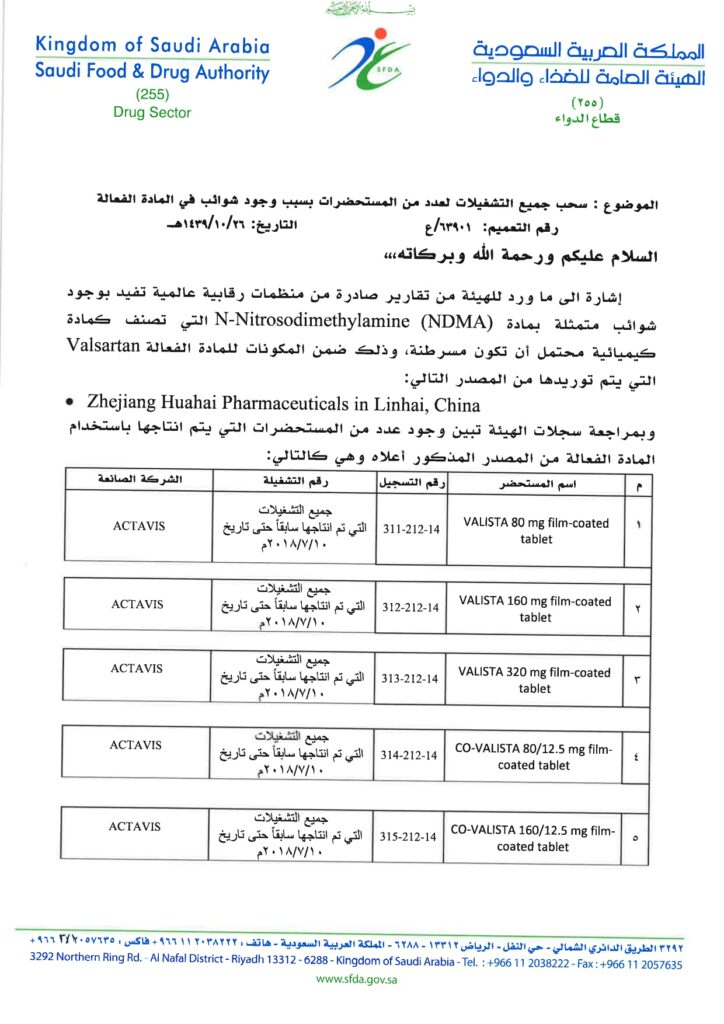
إشارة الى ما ورد للهيئة من تقارير صادرة من منظمات رقابية عالمية تفيد بوجود شوائب متمثلة بمادة N-Nitrosodimethylamine (NDMA) التي تصنف كمادة كيميائية محتمل أن تكون مسرطنة، وذلك ضمن المكونات للمادة الفعالة Valsartan التي يتم توريدها من المصدر التالي:
Zhejiang Huahai Pharmaceuticals in Linhai, China
وبمراجعة سجلات الهيئة تبين وجود عدد من المستحضرات التي يتم انتاجها باستخدام المادة الفعالة من المصدر المذكور أعلاه وهي كالتالي:
| م | اسم المستحضر | رقم التسجيل | رقم التشغيلة | الشركة الصانعة |
| 1 | VALISTA 80 mg film-coated talet | 311-212-14 | جميع التشغيلات التي تم انتاجها سابقاً حتى تاريخ 10-07-2018م | ACTAVIS |
| 2 | VALISTA 160 mg film-coated tablet | 312-212-14 | جميع التشغيلات التي تم انتاجها سابقاً حتى تاريخ 10-07-2018م | ACTAVIS |
| 3 | VALISTA 320 mg film-coated tablet | 312-212-14 | جميع التشغيلات التي تم انتاجها سابقاً حتى تاريخ 10-07-2018م | ACTAVIS |
| 4 | CO-VALISTA 80/12.5 mg film-coated tablet | 314-212-14 | جميع التشغيلات التي تم انتاجها سابقاً حتى تاريخ 10-07-2018م | ACTAVIS |
| 5 | CO-VALISTA 160/12.5 mg film coated tablet | 314-212-14 | جميع التشغيلات التي تم انتاجها سابقاً حتى تاريخ 10-07-2018م | ِِACTAVIS |
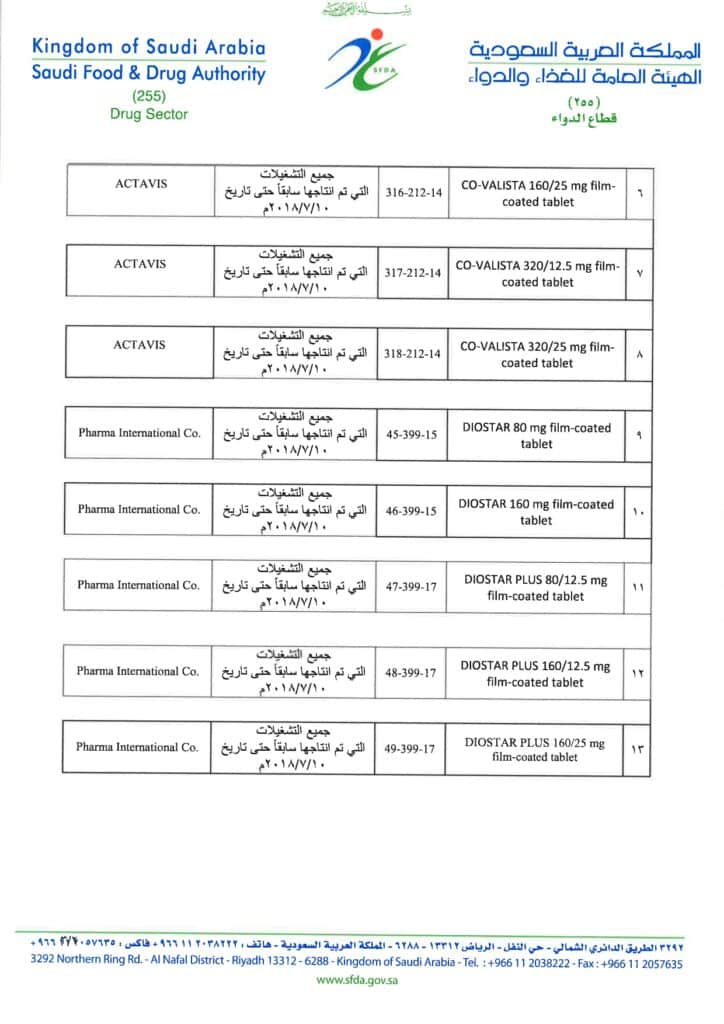
| 6 | CO-VALISTA 160/25 mg film-coated tablet | 316-212-14 | جميع التشغيلات التي تم انتاجها سابقاً حتى تاريخ 10-07-2018م | ACTAVIS |
| 7 | CO-VALISTA 320/12.5 mg film-coated tablet | 317-212-14 | جميع التشغيلات التي تم انتاجها سابقاً حتى تاريخ 10-07-2018م | ACTAVIS |
| 8 | CO-VALISTA 320/25 mg film-coated tablet | 318-212-14 | جميع التشغيلات التي تم انتاجها سابقاً حتى تاريخ 10-07-2018م | ACTAVIS |
| 9 | DIOSTAR 80 mg film-coated tablet | 45-399-15 | جميع التشغيلات التي تم انتاجها سابقاً حتى تاريخ 10-07-2018م | pharma International Co. |
| 10 | DIOSTAR 160 mg film-coated tablet | 46-399-15 | جميع التشغيلات التي تم انتاجها سابقاً حتى تاريخ 10-07-2018م | pharma International Co. |
| 11 | DIOSTAR PLUS 80/12.5 mg film-coated tablet | 47-399-17 | جميع التشغيلات التي تم انتاجها سابقاً حتى تاريخ 10-07-2018م | pharma International Co. |
| 12 | DIOSTAR PlUS 160/12.5 mg film-coated tablet | 48-399-17 | جميع التشغيلات التي تم انتاجها سابقاً حتى تاريخ 10-07-2018م | pharma International Co. |
| 13 | DIOSTAR PlUS 160/25 mg film-coated tablet | 49-399-17 | جميع التشغيلات التي تم انتاجها سابقاً حتى تاريخ 10-07-2018م | pharma International Co. |
لذا نأمل من معاليكم/ سعادتكم التلطف بالاطلاع والتفضل بتوجيه من يلزم حيال إيقاف استخدام المستحضرات المذكورة أعلاه حال وجودها لديكم. علماً بأنه قد تم مخاطبة وكلاء هذه الشركات لإكمال اللازم في القيام بعملية سحب المستحضرات من جميع الجهات المستفيدة.
وتفضلوا بقبول وافر التحية والتقدير،،،
شرح للتعميم وبيانٌ له
لموضوع: سحب مستحضرات Valsartan من الأسواق
الجهة المصدرة: الهيئة العامة للغذاء والدواء
تاريخ الإصدار: 26-10-1439هـ
الموجز:
- المقدمة:
- يشير التعميم إلى تقارير صادرة من منظمات رقابية عالمية تفيد بوجود شوائب متمثلة بمادة N-Nitrosodimethylamine (NDMA) في المادة الفعالة Valsartan.
- تصنف مادة NDMA كمادة كيميائية محتمل أن تكون مسرطنة.
- يتم توريد المادة الفعالة Valsartan من مصدر واحد في الصين.
- أهم القرارات:
- سحب جميع المستحضرات التي تحتوي على المادة الفعالة Valsartan من المصدر المذكور أعلاه من الأسواق.
- إيقاف استخدام هذه المستحضرات حال وجودها لدى الصيدليات أو المستشفيات أو أي جهة أخرى.
- مخاطبة وكلاء الشركات المنتجة لهذه المستحضرات لإكمال عملية السحب من جميع الجهات المستفيدة.
- الهدف من القرار:
- حماية صحة المستهلكين من مخاطر الإصابة بالسرطان.
- ضمان سلامة الأدوية المتداولة في المملكة العربية السعودية.
- ملاحظات:
- هذا التعميم موجه إلى جميع الصيدليات والمستشفيات والجهات الطبية في المملكة العربية السعودية.
ملاحظات إضافية:
- نوع التعميم: تعميم إداري.
- الجهات المستهدفة: جميع الصيدليات والمستشفيات والجهات الطبية في المملكة العربية السعودية.
- الموضوع الرئيسي: سحب مستحضرات Valsartan من الأسواق.
- الهدف من التعميم: حماية صحة المستهلكين من مخاطر الإصابة بالسرطان، وضمان سلامة الأدوية المتداولة في المملكة العربية السعودية.
صورة من التعميم؛ للتحميل